Аналоги Фузеон – отзывы, инструкция
Аналоги Фузеон – отзывы, инструкция
Фузеон
Показания к применению
ВИЧ-1 (в комбинации с др. противоретровирусными ЛС).
Возможные аналоги (заменители)
Действующее вещество, группа
Лекарственная форма
лиофилизат для приготовления раствора для подкожного введения
Противопоказания
Как применять: дозировка и курс лечения
П/к в область плеча, переднюю поверхность бедра или переднюю брюшную стенку. Необходимо менять место каждой последующей инъекции.
Взрослые – 90 мг 2 раза в сутки.
Дети 6-16 лет – 2 мг/кг 2 раза в сутки. Максимальная доза – 90 мг 2 раза в сутки.
Дозы, вводимые 2 раза в сутки и соответствующий объем раствора, рекомендуемые в педиатрической практике в зависимости от массы тела: 11-15.5 кг – 27 мг (0.3 мл), 15.6-20 кг – 36 мг (0.4 мл), 20.1-24.5 кг- 45 мг (0.5 мл), 24.6-29 кг – 54 мг (0.6 мл), 29.1-33.5 кг – 63 мг (0.7 мл), 33.6-38 кг – 72 мг (0.8 мл), 38.1-42.5 кг – 81 мг (0.9 мл), более 42.6 кг – 90 мг (1 мл).
Коррекции дозы для пациентов с КК более 35 мл/мин не требуется.
Лиофилизированный порошок следует разводить стерильной водой для инъекций для получения раствора.
Фармакологическое действие
Ингибитор фузии (слияния). Специфически связываясь с гликопротеидом gp41 ВИЧ-1 вне клетки и ингибируя его структурную реаранжировку, блокирует проникновение вируса внутрь клетки. Не требует внутриклеточной активации. Противовирусная активность обусловлена взаимодействием с др. семикратно повторяющимся участком HR1 в природном gp41 на поверхности вируса.
Побочные действия
Местные реакции: боль, дискомфорт в месте инъекции, уплотнение, эритема, узел, киста, зуд, экхимоз. Редко (1.5%) – абсцесс и флегмона.
Отмечавшиеся не менее чем у 2 взрослых пациентов на 100 пациентов-лет, получавших комбинированное лечение с оптимизированной базовой противоретровирусной терапией.
Со стороны нервной системы: головная боль, периферическая невропатия, головокружение, нарушение вкуса, бессонница, депрессия, тревога, кошмарные сновидения, раздражительность, гипестезия, нарушение концентрации внимания, тремор.
Со стороны дыхательной системы: кашель, боль в горле.
Со стороны кожных покровов: зуд, ночная потливость, сухость кожи, повышенная потливость, себорейная экзема, эритема, акне.
Со стороны опорно-двигательного аппарата: миалгия, артралгия, боль в спине, боли в конечностях, мышечные спазмы.
Со стороны мочевыводящей системы: конкременты в почках, гематурия.
Со стороны пищеварительной системы: тошнота, боль в верхней половине живота, запор, диарея, панкреатит.
Со стороны органов чувств: конъюнктивит, вертиго.
Аллергические реакции: кожная сыпь, зуд, лихорадка, тошнота, рвота, озноб, дрожь, арснижение АД, повышение активности “печёночных” трансаминаз, первичная реакция иммунных комплексов, респираторный дистресс-синдром, гломерулонефрит.
Прочие: слабость, снижение веса, снижение аппетита, анорексия, астения, гриппоподобный синдром, лимфоаденопатия.
Инфекции: кандидоз слизистой ротовой полости, простой герпес, папиллома кожи, грипп, синусит, фолликулит, отит, пневмония.
Лабораторные показатели (изменения наблюдались чаще у пациентов, получавших комбинированную терапию энфувиртидом с оптимизированной базовой противоретровирусной терапией, по сравнению с пациентами, получающими только оптимизированную базовую противоретровирусную терапию): эозинофилия, повышение активности АЛТ, КФК, снижение Hb.
Особые указания
Данные об эффективности препарата у детей старше 3 лет ограничены.
Назначают только в комбинации с др. противоретровирусными ЛС. Пациенты с симптомами предположительной системной аллергической реакции должны прекратить лечение и немедленно пройти медицинское обследование. Не следует возобновлять лечение после возникновения системных реакций, возможно связанных с приемом препарата. Факторы риска, которые могут предопределять развитие или тяжесть аллергической реакции не установлены.
При терапии препаратом отмечена повышенная частота возникновения бактериальной пневмонии (6.6 пациентов с пневмонией по сравнению с 0.6 на 100 пациентов-лет в группах, получавших комбинированную терапию энфувиртидом и оптимизированную базовую противоретровирусную терапию и только оптимизированную базовую терапию, соответственно; в анализ включены бронхопневмония и связанные явления), которая в ряде случаев была фатальной. Частота пневмонии при терапии энфувиртидом была сходной с таковой в общей популяции больных (литературные данные), но была меньше в контрольной группе. Связь пневмонии с терапией препаратом не установлена. Факторы риска для развития пневмонии включают низкое исходное количество CD4+-клеток, высокую вирусную нагрузку, в/в введение ЛС, курение и заболевание легких в анамнезе. Необходимо тщательно контролировать появление симптомов инфекции, особенно, если имеются факторы риска развития пневмонии.
Наиболее частыми побочными явлениями были реакции в месте введения (98%). Но отмена терапии потребовалась только у 4% пациентов. Подавляющее большинство местных реакций (85%) легкой и средней степени тяжести, наблюдается в течение первой недели лечения и не приводит к ограничению обычной деятельности. Степень тяжести болевого синдрома и дискомфорт при продолжении лечения не увеличиваются. Количество местных поражений, наблюдавшихся при запланированном посещении врача во время клинического исследования, составляло менее 5 у 72% пациентов с такими явлениями. Введение препарата лицам, неинфицированным ВИЧ-1 (например, после проведения профилактики) может вызывать появление анти-энфувиртид антител, имеющих перекрёстную реакцию с ВИЧ gp41, что может привести к ложноположительному ВИЧ-тесту при проведении ELISA теста с ВИЧ-антителами.
Энфувиртид не оказывал тератогенного действия в исследованиях, проведённых на животных (крысы и кролики), в дозе в 8.9 раз превышающей терапевтическую для человека. Исследования по применению препарата у беременных женщин не проводились. Применения во время беременности следует избегать, если только потенциальные преимущества терапии для матери не превышают возможный риск для плода.
Неизвестно выделяется ли препарат с грудным молоком у человека,. Кормление грудью следует прекратить до начала терапии, в т.ч. и во избежание передачи ВИЧ ребенку.
Эфувиртид не проявил мутагенных и кластогенных свойств в сериях анализов in vivo и in vitro; не оказывал влияния на фертильность у самцов и самок крыс в дозах, превосходящих в 0.7, 2.5 и 8.3 раз максимальную рекомендованную суточную дозу для человека и рассчитанных в мг/кг п/к.
Не имеется доказательств влияния препарата на способность управлять автомобилем и работать с механизмами, однако необходимо принимать во внимание побочные действия, возникающие при введении препарата.
Разведенный препарат хранят в холодильнике (2-8 град.С) и используют в течение 24 ч. Перед введением готовый раствор из холодильника доводят до комнатной температуры (например, удерживая в руке в течение около 5 мин) и проверяют полностью ли растворилось содержимое флакона. Восстановленный раствор не используют, если он содержит механические включения.
Взаимодействие
Клинически значимых фармакокинетических взаимодействий между энфувиртидом и ЛС, метаболизм которых протекает с участием ферментов семейства CYP450, не установлено.
Введение препарата Фузеон в сочетании с ритонавиром, саквинавиром и рифампицином не приводило к клинически значимым фармакокинетическим взаимодействиям.
Не замещает варфарин, мидазолам, ампренавир или эфавиренз в их местах связывания с белком.
Исследования энфувиртида в комбинации с др. противовирусными средствами различных классов (нуклеозидными ингибиторами обратной транскриптазы, ненуклеозидными ингибиторами обратной транскриптазы и ингибиторами протеаз), включая зидовудин, ламивудин, нелфинавир, индинавир и. эфавиренз, показали наличие от аддитивного до синергичного эффектов и отсутствие антагонизма. Взаимосвязи между чувствительностью ВИЧ-1 к энфурвитиду in vitro и ингибированием репликации ВИЧ-1 у человека не установлено. Из-за различных ферментов-мишеней и как предполагается за счёт активности энфувиртида в отношении ВИЧ-штаммов, устойчивых к др. классам противовирусных средств, ВИЧ-изоляты, устойчивые к энфувиртиду должны оставаться чувствительными к нуклеозидным ингибиторам обратной транскриптазы, ненуклеозидным ингибиторам обратной транскриптазы и ингибиторам протеаз.
Не следует смешивать с др. ЛС, за исключением поставляемого растворителя (вода для инъекций).
Фузеон
Курс лечения препаратом Фузеон назначает врач. Для этого вы должны обратиться в больницу за его консультацией.
Как препарат выпускается
лиофилизат для приготовления раствора для подкожного введения 90мг/мл
Кто препарат изготавливает
Рош Диагностикс ГмбХ (Германия)
Хоффманн-Ля Рош Лтд (Швейцария)
Фарм. группа
Из чего производится (состав)
Международное наименование
Фармакологическое действие
Ингибитор фузии (слияния). Не требует внутриклеточной активации. Противовирусная активность обусловлена взаимодействием с др. семикратно повторяющимся участком HR1 в природном др41 на поверхности вируса. Абсорбция не зависит от места введения. Являясь пептидом, подвергается катаболизму до аминокислот, входящих в его состав, с последующей их утилизацией в организме. Не ингибирует ферменты семейства цитохрома CYP450. Фармакокинетика энфувиртида у пациентов с печёночной и почечной недостаточностью не изучалась, а также у пациентов в возрасте старше 65 лет.
Показания к назначению
ВИЧ-1 (в комбинации с др. противоретровирусными ЛС).
Противопоказания к применению
Гиперчувствительность, лактация. С осторожностью: беременность, детский возраст (до 6 лет).
Побочные действия лекарства
Местные реакции: боль, дискомфорт в месте инъекции, уплотнение, эритема, узел, киста, зуд, экхимоз. Со стороны нервной системы: головная боль, периферическая невропатия, головокружение, нарушение вкуса, бессонница, депрессия, тревога, кошмарные сновидения, раздражительность, гипестезия, нарушение концентрации внимания, тремор. Со стороны дыхательной системы: кашель, боль в горле. Со стороны кожных покровов: зуд, ночная потливость, сухость кожи, повышенная потливость, себорейная экзема, эритема, акне. Со стороны опорно-двигательного аппарата: миалгия, артралгия, боль в спине, боли в конечностях, мышечные спазмы. Со стороны мочевыводящей системы: конкременты в почках, гематурия. Со стороны пищеварительной системы: тошнота, боль в верхней половине живота, запор, диарея, панкреатит. Со стороны органов чувств: конъюнктивит, вертиго. Аллергические реакции: кожная сыпь, зуд, лихорадка, тошнота, рвота, озноб, дрожь, арснижение АД, повышение активности “печёночных” трансаминаз, первичная реакция иммунных комплексов, респираторный дистресс-синдром, гломерулонефрит. Прочие: слабость, снижение веса, снижение аппетита, анорексия, астения, гриппоподобный синдром, лимфоаденопатия. Инфекции: кандидоз слизистой ротовой полости, простой герпес, папиллома кожи, грипп, синусит, фолликулит, отит, пневмония. Лабораторные показатели: эозинофилия, повышение активности АЛТ, КФК, снижение Нb.
Взаимодействие
Клинически значимых фармакокинетических взаимодействий между энфувиртидом и ЛС, метаболизм которых протекает с участием ферментов семейства CYP450, не установлено. Введение препарата Фузеон в сочетании с ритонавиром, саквинавиром и рифампицином не приводило к клинически значимым фармакокинетическим взаимодействиям. Энфувиртид не вытесняется из мест своего связывания с белком саквинавиром, нелфинавиром, лопинавиром, эфавирензом, невирапином, ампренавиром, итраконазолом, мидазоламом или варфарином. Не замещает варфарин, мидазолам, ампренавир или эфавиренз в их местах связывания с белком. Исследования энфувиртида в комбинации с др. противовирусными средствами различных классов (нуклеозидными ингибиторами обратной транскриптазы, ненуклеозидными ингибиторами обратной транскриптазы и ингибиторами протеаз), включая зидовудин, ламивудин, нелфинавир, индинавир и эфавиренз, показали наличие от аддитивного до синергичного эффектов и отсутствие антагонизма. Взаимосвязи между чувствительностью ВИЧ-1 к энфурвитиду in vitro и ингибированием репликации ВИЧ-1 у человека не установлено. Из-за различных ферментов-мишеней и как предполагается за счёт активности энфувиртида в отношении ВИЧ-штаммов, устойчивых к др. классам противовирусных средств, ВИЧ-изоляты, устойчивые к энфувиртиду должны оставаться чувствительными к нуклеозидным ингибиторам обратной транскриптазы, ненуклеозидным ингибиторам обратной транскриптазы и ингибиторам протеаз. Не следует смешивать с др. ЛС, за исключением поставляемого растворителя (вода для инъекций).
Возможные дозы препарата
П/к в область плеча, переднюю поверхность бедра или переднюю брюшную стенку. Необходимо менять место каждой последующей инъекции. Взрослые – 90 мг 2 раза в сутки. Дети 6-16 лет – 2 мг/кг 2 раза в сутки. Максимальная доза – 90 мг 2 раза в сутки. Дозы, вводимые 2 раза в сутки и соответствующий объем раствора, рекомендуемые в педиатрической практике в зависимости от массы тела: 11-15.5 кг – 27 мг (0.3 мл), 15.6-20 кг – 36 мг (0.4 мл), 20.1-24.5 кг – 45 мг (0.5 мл), 24.6-29 кг – 54 мг (0.6 мл), 29.1-33.5 кг – 63 мг (0.7 мл), 33.6-38 кг – 72 мг (0.8 мл), 38.1-42.5 кг – 81 мг (0.9 мл), более 42.6 кг – 90 мг (1 мл). Коррекции дозы для пациентов с КК более 35 мл/мин не требуется. Лиофилизированный порошок следует разводить стерильной водой для инъекций для получения раствора.
Превышение дозы лекарства
Симптомы: усиление побочных эффектов. Лечение: симптоматическое. Специфического антидота нет.
Особые рекомендации по применению препарата
Данные об эффективности препарата у детей старше 3 лет ограничены. Назначают только в комбинации с др. противоретровирусными ЛС. Пациенты с симптомами предположительной системной аллергической реакции должны прекратить лечение и немедленно пройти медицинское обследование. Не следует возобновлять лечение после возникновения системных реакций, возможно связанных с приемом препарата. Факторы риска, которые могут предопределять развитие или тяжесть аллергической реакции не установлены. При терапии препаратом отмечена повышенная частота возникновения бактериальной пневмонии. Необходимо тщательно контролировать появление симптомов инфекции, особенно, если имеются факторы риска развития пневмонии. Введение препарата лицам, неинфицированным ВИЧ-1 может вызывать появление анти-энфувиртид антител, имеющих перекрёстную реакцию с ВИЧ gp41, что может привести к ложноположительному ВИЧ-тесту при проведении ELISA теста с ВИЧ-антителами.
Метод хранения и условия
Хранить при температуре не выше 30 град. С – лиофилизат; при температуре 2-8 град. – восстановленный раствор.
Способ реализации
Отпускается по рецепту
Внимание. Приментять препарат следует только после получения назначения у врача.
Фузеон – официальная инструкция по применению
Регистрационный номер
Торговое наименование
Международное непатентованное наименование
Лекарственная форма
Лиофилизат для приготовления раствора для подкожного введения
Состав
1 флакон с препаратом содержит:
активное вещество: энфувиртид – 108 мг;
вспомогательные вещества: натрия карбонат (безводный) – 2.87 мг, маннитол – 27.05 мг, натрия гидроксид – q.s., хлористоводородная кислота – q.s.
1 флакон с растворителем содержит: вода для инъекций – 2 мл.
Описание
Лиофилизат белого или белого со слегка желтоватым оттенком цвета.
Растворитель: прозрачная бесцветная жидкость.
Восстановленный раствор: прозрачный, бесцветный или слегка желтоватого цвета раствор.
Фармакотерапевтическая группа
Противовирусное [ВИЧ] средство
Код АТХ [J05AX07]
Фармакологические свойства
Фармакодинамика
Энфувиртид – первый представитель класса терапевтических средств, называемых ингибиторами слияния. Специфически связываясь с гликопротеидом gp41 вируса иммунодефицита человека 1 (ВИЧ-1) вне клетки и ингибируя его структурную реаранжировку, блокирует проникновение вируса внутрь клетки. Не требует внутриклеточной активации. Противовирусная активность энфувиртида обусловлена его взаимодействием с первым участком, содержащим гептадные повторы (HR1) в природном gp41 на поверхности вируса.
Противовирусная активность in vitro: была продемонстрирована с использованием лабораторных и клинических ВИЧ-1 изолятов на примере острой инфекции в культуре клеток Т-лимфобластов, клеток моноцитов/макрофагов и первичных мононуклеаров периферической крови (ПМПК). Выявлена селективная анти-ВИЧ-1 активность как в отношении прототипных, так и в отношении первичных вирусных изолятов. При определении чувствительности к энфувиртиду на 612 рекомбинантных образцах ВИЧ, содержащих env гены рибонуклеиновой кислоты (РНК) вируса, с помощью рекомбинантного метода фенотипирования с использованием переноса ВИЧ среднее геометрическое ЕС50 (концентрация, при которой достигается половина максимального эффекта) энфувиртида составляло 0.259 мкг/мл (среднее геометрическое ± 2SD = 1.96, мкг/мл). Данные образцы были получены до начала терапии у пациентов, участвовавших в клинических исследованиях III фазы.
Исследования энфувиртида в комбинации с другими противовирусными средствами различных классов (нуклеозидными ингибиторами обратной транскриптазы, ненуклеозидными ингибиторами обратной транскриптазы и ингибиторами протеаз), включая зидовудин, ламивудин, нелфинавир, индинавир и эфавиренз, показали наличие аддитивного и синергичного эффектов и отсутствие антагонизма. Взаимосвязи между чувствительностью ВИЧ-1 к энфувиртиду in vitro и ингибированием репликации ВИЧ-1 у человека не установлено. Из-за различных ферментов-мишеней и, как предполагается, за счет активности энфувиртида в отношении ВИЧ штаммов, устойчивых к другим классам противовирусных средств, ВИЧ изоляты, устойчивые к энфувиртиду, должны оставаться чувствительными к нуклеозидным ингибиторам обратной транскриптазы, ненуклеозидным ингибиторам обратной транскриптазы и ингибиторам протеаз.
Резистентность in vitro: выделены ВИЧ-1 изоляты со сниженной чувствительностью к энфувиртиду и заменами в последовательности аминокислот (аа) 36-38 эктодомена gp41.
Эти замены коррелировали с различными уровнями сниженной чувствительности к энфувиртиду ВИЧ-мутантов с сайт-направленными мутациями. Резистентность in vivo: в клинических исследованиях III фазы ВИЧ рекомбинанты, содержащие env гены РНК ВИЧ из образцов, полученных у 187 пациентов на 24 неделе лечения, продемонстрировали более чем 4-кратное снижение чувствительности к энфувиртиду по сравнению с образцами, взятыми до начала терапии. Из исследованных в данном эксперименте образцов 185 (98.9%) содержали специфические замены в аа 36-45 gp41 вирусов. Эти замены, возникавшие с уменьшающейся частотой, происходили в аа в положениях 38, 43, 36, 40, 42 и 45.
Специфичные единичные замены в аминокислотных остатках gp41 в разной степени приводили к снижению вирусной чувствительности к энфувиртиду по сравнению с исходным уровнем. Отклонения от показателя среднего геометрического для чувствительности колебались от 15.2-кратного снижения для V38M до 41.6-кратного снижения для V38A. Недостаточное количество образцов, содержащих множественные замены, не позволяет отследить закономерность этих замен, равно как и их воздействие на вирусную чувствительность к энфувиртиду. Взаимосвязь этих замен с эффективностью in vivo не установлена. Степень снижения вирусной чувствительности к энфувиртиду коррелировала с устойчивостью к базовой антиретровирусной терапии до инициации лечения (см. Таблица 1).
Перекрестная резистентность: благодаря новой вирусной мишени энфувиртид одинаково активен in vitro в отношении диких типов лабораторных изолятов, клинических изолятов и изолятов с генотипической устойчивостью к 1, 2 или 3 классу противовирусных средств (нуклеозидным ингибиторам обратной транскриптазы, ненуклеозидным ингибиторам обратной транскриптазы и ингибиторам протеаз). И, наоборот, предполагается, что мутации в gp41 аа 36-45, которые вызывают устойчивость к энфувиртиду, не должны вызывать перекрестной чувствительности к другим классам антиретровирусных средств.
Через 48 недель терапии неопределяемый уровень РНК ВИЧ-1 (менее 400 копий/мл) отмечен у 30% пациентов, получавших Фузеон® в комбинации с оптимизированной базовой (ОБ) антиретровирусной терапией (АРТ), по сравнению с 12% у пациентов, получавших только оптимизированную базовую АРТ. Более часто неопределяемый уровень РНК ВИЧ-1 отмечен у всех пациентов при терапии препаратом Фузеон®, независимо от исходного уровня РНК ВИЧ-1, количества CD4 клеток, числа предшествующих или получаемых в настоящий момент компонентов АРТ. В то же время у пациентов с количеством CD4 более 100 клеток/мл, исходной вирусной нагрузкой менее 5 log10 копий/мл, получавших ранее менее 10 препаратов АРТ и 1 или более препаратов, входящих в ОБ в настоящее время, было больше шансов достичь неопределяемого уровня РНК ВИЧ-1 (см. Таблица 1).
Фузеон® в комбинации с оптимизированным базовым лечением при сравнении с применением только базовой терапии у ВИЧ-1 инфицированных пациентов достоверно лучше и статистически значимо изменял уровни РНК ВИЧ-1 в плазме в log10 копий/мл (-1.5 против -0.6), количество CD4 клеток (+91 против +45), процент пациентов со снижением РНК ВИЧ в ?1 log и более по сравнению с исходным уровнем (37% против 17%), 1 log10 РНК ВИЧ-1 и у 29% пациентов уровень РНК ВИЧ-1 был ниже 400 копий/мл. Средние изменения РНК ВИЧ-1 и количества CD4 клеток составляли 1.24 log10 копий/мл и 237 клеток/мкл, соответственно.
Данные доклинического изучения безопасности
Канцерогенез: долговременные исследования канцерогенности энфувиртида на животных не проводились.
Мутагенез: энфувиртид не проявил мутагенных и кластогенных свойств в сериях анализов in vivo и in vitro, включая Ames тест обратной мутации в бактериях, анализ ранней генной мутации в линии AS52 клеток яичника китайского хомячка и in vivo микронуклеарный анализ на мышах.
Нарушение фертильности: энфувиртид не оказывал нежелательных эффектов на фертильность у самцов и самок крыс в дозах, превосходящих в 0.7, 2.5 и 8.3 раз максимальную рекомендованную суточную дозу для человека и рассчитанных в мг/кг подкожно.
Фармакокинетика
После однократного подкожного (п/к) введения в область передней брюшной стенки 90 мг энфувиртида ВИЧ-1 инфицированным пациентам максимальная концентрация (Сmax) составляет 4.59±1.5 мкг/мл, площадь под кривой «концентрация – время» (AUC) – 55.8±12.1 мкг x ч/мл и абсолютная биодоступность 84.3±15.5%. При п/к введении в дозе от 45 до 180 мг биодоступность энфувиртида пропорциональна вводимой дозе. Абсорбция не зависит от места введения.
Средняя равновесная концентрация в плазме при введении 90 мг энфувиртида представлена на Рисунке 1.
Рисунок 1. Равновесная концентрация в плазме при введении 90 мг энфувиртида* два раза в сутки (N=11)
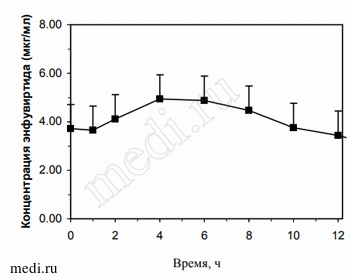
* Полоса ошибки = стандартное отклонение
Средняя минимальная равновесная концентрация энфувиртида в плазме между двумя введениями 2.6-3.4 мкг/мл.
Средний объем распределения при равновесном состоянии после внутривенного введения 90 мг составляет 5.5+1.1 л. В ВИЧ-инфицированной плазме энфувиртид в концентрации от 2-10 мкг/мл на 92% связан с белками плазмы, в основном с альбумином и в меньшей степени с a1-кислым гликопротеином.
У ВИЧ-инфицированных пациентов уровень содержания энфувиртида в спинномозговой жидкости незначителен. Вероятно, молекулы препарата слишком велики для преодоления гематоэнцефалического барьера.
Энфувиртид, являясь пептидом, подвергается катаболизму до аминокислот, входящих в его состав, с последующим метаболизмом последних в организме.
Энфувиртид не является ингибитором ферментов семейства цитохрома CYP450. In vitro гидролиз амидной группы С-конца аминокислоты фенилаланина приводит к образованию дезаминированного метаболита и образование этого метаболита не зависит от НАДФН. Этот метаболит обнаруживается в плазме человека после введения энфувиртида с AUC 2.4-15% от AUC энфувиртида.
Меченный 3Н-энфувиртид не полностью обнаруживается в экскрементах грызунов в течение 7 дней после введения дозы. Задержка радиоактивности отмечена в скелетных мышцах.
После подкожного введения 90 мг энфувиртида период полувыведения равен 3.8±0.6 ч, а клиренс составляет 1.7±0.4 л/ч.
Фармакокинетика у особых групп пациентов
Пациенты с печеночной недостаточностью: фармакокинетика энфувиртида у пациентов с печеночной недостаточностью не изучалась.
Пациенты с почечной недостаточностью: анализ плазменных концентраций у пациентов в клинических исследованиях показал, что клиренс энфувиртида не демонстрировал зависимости от клиренса креатинина у пациентов с клиренсом креатинина более 35 мл/мин.
По данным клинического исследования, посвященного изучению пациентов с почечной недостаточностью, клиренс энфувиртида снижался на 38% у пациентов с тяжелым нарушением функции почек и на 14-28% – у пациентов с терминальной стадией почечной недостаточности, находящихся на диализе, а AUC энфувиртида увеличивалась в среднем на 43-62% в обеих группах по сравнению с пациентами с нормальной функцией почек. Полученные результаты находились в пределах, которые были зафиксированы в рамках широкомасштабных исследований, проводившихся на пациентах с нормальной функцией почек. Гемодиализ не влиял существенно на клиренс энфувиртида. Коррекции дозы для пациентов с нарушениями функции почек не требуется.
Пол и масса тела: клиренс энфувиртида на 20% ниже у женщин, чем у мужчин и увеличивается с увеличением массы тела независимо от пола (на 20% выше у пациентов с массой тела 100 кг и на 20% ниже у пациентов с массой тела 40 кг относительно пациента сравнения с массой тела 70 кг). Эти изменения не являются клинически значимыми и не требуют коррекции дозы.
Раса: не выявлено расовых различий клиренса препарата между представителями негроидной, монголоидной расы по сравнению с представителями европеоидной расы после соответствующей коррекции воздействия с учетом массы тела.
Пациенты старческого возраста: фармакокинетика энфувиртида у пациентов в возрасте 65 лет и старше не изучалась.
у детей от 3-х до 16 лет при назначении в дозе 2 мг/кг два раза в сутки (не более 90 мг два раза в сутки) отмечена концентрация энфувиртида в плазме, аналогичная той, которая достигается у взрослых пациентов, получавших препарат в дозе 90 мг два раза в сутки.
У детей в возрасте от 5 и до 16 лет, получавших энфувиртид в дозе 2 мг/кг два раза в сутки, AUC в равновесном состоянии составляет 54.3±23.5 мкг.ч/мл, Сmax – 6.14±2.48 мкг/мл и Сmin между введениями составляет 2.93±1.55 мкг/мл.
Показания к применению
Лечение ВИЧ-1 инфекции в комбинации с другими антиретровирусными препаратами при неэффективности режимов предыдущей терапии, содержащих как минимум один из препаратов каждой следующей группы: ингибиторы протеазы, нуклеозидные ингибиторы обратной транскриптазы, ненуклеозидные ингибиторы обратной транскриптазы или при непереносимости ранее применяемых режимов антиретровирусной терапии.
Противопоказания
Гиперчувствительность к энфувиртиду или к любому компоненту препарата. Период грудного вскармливания. Дети с массой тела менее 11 кг.
Применение при беременности и в период грудного вскармливания
Энфувиртид не оказывал тератогенного действия в исследованиях, проведенных на животных (крысы и кролики), в дозе в 8.9 раз превышающей терапевтическую для человека. Исследования по применению препарата Фузеон® у беременных женщин не проводились. Применения препарата Фузеон® во время беременности следует избегать. Применение возможно только в том случае, если потенциальная польза для матери превышает возможный риск для плода.
При введении радиомеченного Н3-энфувиртида крысам в период лактации в молоке присутствует очень низкий уровень радиоактивности. Выделяется ли энфувиртид с грудным молоком у человека, неизвестно. Кормление грудью следует прекратить до начала терапии, в т.ч. и во избежание передачи ВИЧ ребенку.
Способ применения и дозы
Стандартный режим дозирования
Ежедневно, подкожно (п/к) в область плеча, переднюю поверхность бедра или переднюю брюшную стенку. Необходимо менять место каждой последующей инъекции и вводить препарат туда, где в настоящее время нет местной реакции на инъекцию. Взрослые и дети старше 16 лет: по 90 мг два раза в сутки.
Дозирование в особых случаях
Дети до 6 лет: данные для определения рекомендаций по режиму дозирования препарата Фузеон® у детей в возрасте до 6 лет ограничены.
Дети 6-16 лет: по 2 мг/кг два раза в сутки. Максимальная доза по 90 мг два раза в сутки (см. Таблица 2).
Таблица 2. Дозы, рекомендуемые в педиатрической практике.
Источники:
http://www.webapteka.ru/drugbase/name18568.html
http://2glazza.ru/content/fuzeon
http://medi.ru/instrukciya/fuzeon_14858/